Forskjell mellom dietyleter og petroleumseter | Diethyl Ether vs Petroleum Ether
Nøkkelforskjell - Diethyleter vs Petroleumeter
Selv om de to navnene dietyleter og petroleumeter høres ganske likt, er de helt forskjellige kjemiske forbindelser med mange industrielle anvendelser. Dietyleter er en ren organisk væske og petroleumeter er en blanding av hydrokarboner. Hovedforskjellen mellom dietyleter og petroleumseter er at dietyleter er en eter mens petroleumeter ikke inneholder en eterbinding (-O-). De finnes begge i flytende form ved romtemperatur med svært flyktige egenskaper.
Hva er dietyleter?
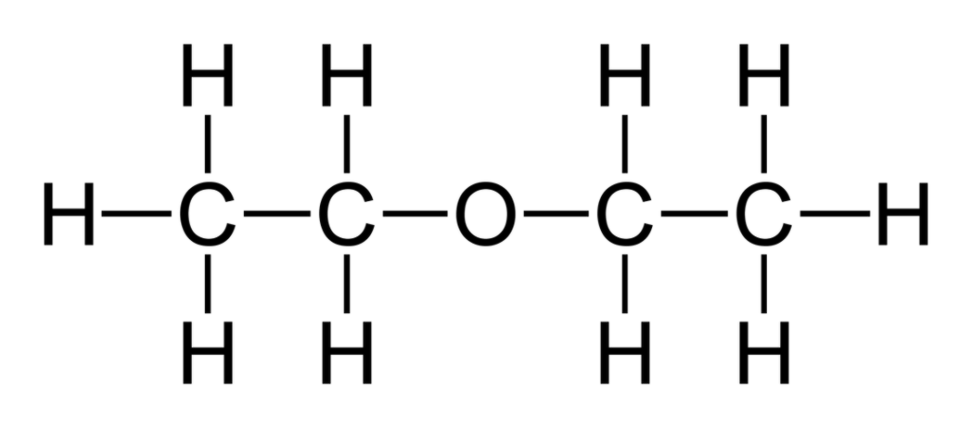
Dietyleter, også kjent som etyleter , er en organisk forbindelse med en sterk karakteristisk lukt og en varm, søt smak. Molekylformelen og molekylvekten av dietyleter er henholdsvis C 4 H 10 O og 74. 1216 g mol -1 . Det er et fargeløst, svært flyktig, brennbart (kokepunkt 34. 5 ° C [94. 1 ° F]) væske. Den molekylære strukturen har to etylgrupper (-CH 2
CH 3 ) koblet gjennom et oksygenatom (C 2 H 5 OC 2 H 5 ).
0 C. Dens tetthet er lavere enn tettheten av vann og det er vannløselig; det flyter på vann. Det er noen ganger referert til som
bensin, bensin, petroleum bensin, canadol, lys ligroin
og skellysolve .
Egenskaper av dietyleter og petroleumeter: Dietyleter: Dietyleter er en fargeløs, svært flyktig væske med en søt, skarp lukt. Det er litt løselig i vann og mindre tett enn vann. Dampen er tyngre enn luften. Dietyleter er relativt polært molekyl og det kan danne hydrogenbindinger med vann.

Petroleumeter:
Petroleumeter er en klar, fargeløs, flyktig væske med lukten av hydrokarboner.Det er vannuopløselig og mindre tett enn vann; dermed flyter det på vann. Petroleumeter er en ikke-polar forbindelse, derfor er den uoppløselig i polare løsemidler.
Bruk av dietyleter og petroleumeter: Dietyleter:
Dietyleter brukes i næringer for å lage andre kjemikalier og i biomedisinsk forskning. Det er et velkjent bedøvelsesmiddel og mye brukt som løsningsmiddel. Det brukes vanligvis som et løsningsmiddel for voks, fett, oljer, parfymer, alkaloider og tannkjøtt. Petroleumeter:
Petroleumseter brukes som løsemiddel, drivstoff, vaskemiddel og som insektmiddel. Det brukes som løsemiddel for oljer, fett og voks. Den brukes også i fotografering, maling og lakk.
Helseeffekter av dietyleter og petroleumeter: Dietyleter:
Innånding av dietyleterdamp kan forårsake kvalme, hodepine, oppkast og bevissthetstap. Øyekontakt kan forårsake irritasjon og hudkontakt med våte klær kan forårsake brannskader. Petroleumeter:
De vanligste måtene for eksponering av petroleumeter kan skje ved innånding og hudkontakt. Over eksponering er skadelig og det bringer flere helseeffekter i menneskekroppen. Alvorlige effekter kan forårsake hvis den inneholder en høyere konsentrasjon av aromatiske hydrokarboner. For eksempel påvirker innånding sentralnervesystemet (CNS) som forårsaker hodepine, svimmelhet, kvalme, tretthet og inkoordinering. Hudkontakt kan forårsake hudallergi og oral inntak forårsaker irritasjon i slimhinnen, oppkast, og depresjon i sentralnervesystemet.
Definisjoner: Løsemiddel: Et løsemiddel er et stoff som kan oppløse andre stoffer.
Flyktig: Fordampes enkelt ved normale temperaturer Brannfarlig: Lett å sette i brann
Referanser:
Åpne kjemedatabase. (2016). Nasjonalt institutt for helse. Hentet 11. april, 2016, herfra
Biologiske effekter av eksponering. (2016). Sentre for sykdomskontroll og forebygging. Hentet 11. april, 2016, herfra
Bilde Courtesy:
"Diethyl-ether-2D-flat" (Public Domain) via Commons Wikimedia
"Petroleumeter" av Seilvorbau - eget arbeid (CC BY-SA 4. 0) via Wikimedia Commons



