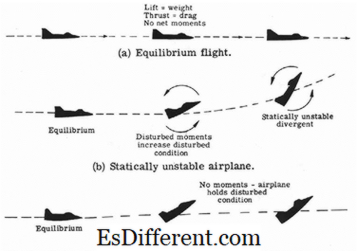
Forskjell mellom fenyl og benzyl | Fenyl vs benzyl
fenyl vs benzyl
Både fenyl og benzyl er avledet fra benzen, og forveksles ofte av studenter i kjemi. Fenyl er et hydrokarbonmolekyl med formelen C 6 H 5 , mens benzyl er C 6 H 5 CH 2 <; en ekstra CH 2 gruppe festet til benzenringen. Fenyl
Fenyl er et hydrokarbonmolekyl med formelen C

H 5 . Dette er avledet fra benzen, derfor har lignende egenskaper som benzen. Dette er imidlertid forskjellig fra benzen på grunn av mangel på et hydrogenatom i ett karbon. Så molekylvekten av fenyl er 77 g mol -1 . Fenyl er forkortet som Ph. Vanligvis er fenyl festet til en annen fenylgruppe, atom eller molekyl (denne delen er kjent som substituenten, R-gruppen som i figuren). Karbonatomer av fenyl er sp2 hybridisert som i benzen. Alle karbonene kan danne tre sigma-bindinger. To av sigma-bindingene dannes med to tilstøtende karboner, slik at det vil gi opphav til en ringstruktur. Det andre sigmabindingen er dannet med et hydrogenatom. Imidlertid, i et karbon i ringen, dannes det tredje sigma-bindingen med et annet atom eller molekyl snarere enn et hydrogenatom. Elektronene i p-orbitaler overlapper hverandre for å danne den delokaliserte elektronmolen. Derfor har fenyl lignende C-C bindingslengder mellom alle karboner, uavhengig av å ha vekslende enkelt- og dobbeltbindinger. Denne C-C bindelengden er ca. 1, 4 Å. Ringen er plan og har en 120 ° vinkel mellom bindinger rundt et karbon. På grunn av substituentgruppen av fenyl, endres polariteten og andre kjemiske eller fysiske egenskaper. Hvis substituenten donerer elektroner til den delokaliserte elektronmolen i ringen, er de kjent som elektrondonerende grupper (E.g.-OCH 3 , NH 2 ). Hvis substituenten tiltrekker elektroner fra elektronskyen, er den kjent som elektron-uttrekkende substituent. (E. g. -NO 2 , -COOH). Fenylgrupper er stabile på grunn av deres aromatiske egenskaper, slik at de ikke lett gjennomgår oksidasjoner eller reduksjoner. Videre er de hydrofobe og ikke-polare. Benzyl Formelen av benzyl er C
6H
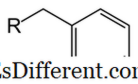
5 CH 2 . Dette er også et derivat av benzen. Sammenlignet med fenyl har benzyl en CH 2 gruppe festet til benzenringen. En annen molekylær del (R-gruppe som vist på bildet) kan bindes til benzylgruppen via binding til CH 2 karbonatomet. Benzylgruppe er forkortet som "Bn". Molekylvekten til benzylgruppen er 91 g mol -1 . Siden det er en benzenring, er benzylgruppen aromatisk.I organiske kjemimekanismer kan benzylgruppen dannes enten som en radikal karbokalisering (C 6 H 5 CH 2 + ) eller en karboksion (C 6 H 5 CH 2 - ). For eksempel, i nukleofile substitusjonsreaksjoner, dannes benzylisk radikal eller kation-mellomprodukt. Det er en høyere stabilisering av disse mellomproduktene sammenlignet med alkylradikal eller kation. Reaktiviteten til benzylstilling er lik den for allyliske posisjon. Benzylgrupper brukes ofte i organisk kjemi som beskyttende grupper, spesielt for å beskytte karboksylsyre eller alkoholfunksjonelle grupper.
H
5 CH < 2 . • Benzyl har ekstra CH 2 gruppe sammenlignet med fenyl. • I fenyl er bensenringen direkte knyttet til et substituentmolekyl eller et atom, men i benzyl, gjør CH 2 gruppen forbindelse med et annet molekyl eller et atom.