Forskjell mellom lysin og L-lysin | Lysin vs L-lysin
Hovedforskjell - Lysin vs L-lysin
Lysin og L-lysin er begge typer aminosyrer og deler samme fysiske egenskaper, men det er noen forskjell mellom dem. nøkkelforskjellen mellom lysin og L-lysin er i evnen til å rotere planpolarisert lys. Lysin er en biologisk aktiv naturlig forekommende essensiell a-aminosyre. Det kan forekomme i to isomere former på grunn av muligheten til å danne to forskjellige enantiomerer rundt det chirale karbonatomet. Disse er kjent som L- og D-former, analoge med venstrehånds og høyrehånds konfigurasjoner. Disse L- og D-formene sies å være optisk aktive og rotere planpolarisert lys i en annen forstand; med klokken eller mot urviseren. Hvis lyset roterer lysin mot urviseren, viser lyset levorotasjon, og det er kjent som L-lysin. Det skal imidlertid nøye noteres her at D- og L-merking av isomerene ikke er det samme som d- og l-merkingen.
Hva er Lysine?
Lysin er en essensiell aminosyre som er ikke syntetisert i kroppen vår og må leveres av den vanlige dietten. Derfor er lysin en essensiell aminosyre for mennesker. Det er en biologisk viktig organisk forbindelse sammensatt av amin (-NH 2 ) og karboksylsyre (-COOH) funksjonelle grupper med kjemisk formel NH 2 - (CH 2) 4 -CH (NH 2 ) - COOH. Nøkkelelementene i lysin er karbon, hydrogen, oksygen og nitrogen. I biokjemi er aminosyrer som har både aminen og karboksylsyregruppene knyttet til det første (a-a) karbonatom kjent som a-aminosyrer . Derfor anses lysin også som a-aminosyrer. Strukturen av lysin er gitt i figur 1. Figur 2: Molekylær struktur av lysin (* karbonatom er et chiralt eller asymmetrisk karbonatom og representerer også alfa-karbonatomet) Lysin er grunnleggende i naturen fordi den inneholder to basiske amino grupper og en sur karboksylsyregruppe. Derfor danner det også omfattende hydrogenbinding på grunn av tilstedeværelsen av to aminogrupper.
Gode kilder til lysin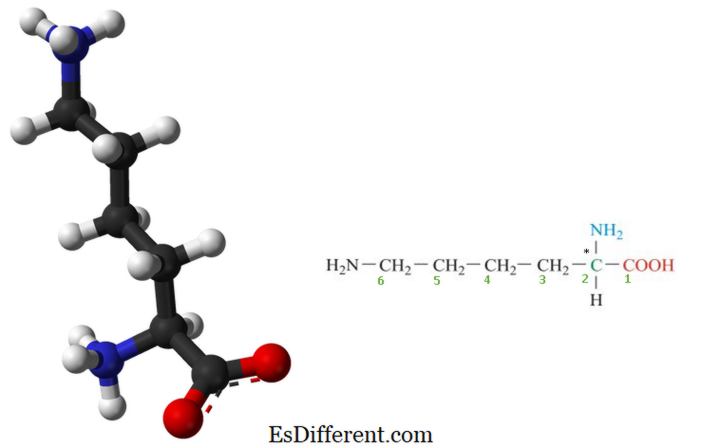
er proteinrike dyrekilder som
egg, rødt kjøtt, lam, svin og fjærfe, ost og fisk (som torsk og sardiner). Lysin er også rik på planteproteiner som soya, bønner og erter. Det er imidlertid en begrensende aminosyre i de fleste kornkorn, men er rikelig i de fleste pulser og belgfrukter.
karbon, og det er
asymmetrisk struktur .Lysin er også en optisk aktiv aminosyre på grunn av tilstedeværelsen av dette asymmetriske eller chirale karbonatom. Lysin kan således skape stereoisomerer som er isomere molekyler som har samme molekylformel, men varierer i de tredimensjonale orienteringene av atomene deres i rommet. Enantiomerer er to stereoisomerer som er relatert til hverandre av en refleksjon, eller de er speilbilder av hverandre som ikke er overordnede. Lysin er tilgjengelig i to enantiomere former kjent som L- og D- og enantiomerene av lysin er gitt i figur 2. Figur 2: Enantiomerer av lysinaminosyre. Gruppene COOH, H, R og NH2 er anordnet rundt C-atomet i en retning med urviseren, og enantiomeren kalles for eksempel L-form og D-form. L- og D-bare refererer til romlige arrangement rundt karbonatomet og refererer ikke til optisk aktivitet. Mens L- og D-formene til et chiralt molekyl roterer planet av polarisert lys i forskjellige retninger, roterer noen L-former (eller D-former) lys til venstre (levo eller l-form) og noen til høyre (dextro eller d-form). l- og d-former kalles optiske isomerer. L-lysin og D-lysin er enantiomerer av hverandre har de samme fysiske egenskaper, bortsett fra retningen der de roterer polarisert lys. De har ikke-overlegne speilbildeforhold. Nomenklaturen til D og L er imidlertid ikke vanlig i aminosyrer, inkludert lysin. De roterer det plane polariserte lyset i samme størrelsesorden, men i forskjellige retninger. D- og L-isomeren av lysin som roterer det polariserte polariserte lyset i retning med urviseren kalles som dextrorotatorisk eller d-lysin
 , og den som roterer det polariserte polariserte lyset mot urviseren, kalles laevorotatorisk eller
, og den som roterer det polariserte polariserte lyset mot urviseren, kalles laevorotatorisk eller
L-lysin (Figur 2). L-Lysin er mest tilgjengelige stabile form av lysin . D-Lysin er en syntetisk form av lysin og kan syntetiseres fra l-lysin ved rasemisering. Det benyttes i behandlingen av poly-d-lysin, som brukes som et beleggmateriale for å forbedre cellevedlegget. L-lysin spiller en betydelig rolle i menneskekroppen, i kalsiumabsorpsjon, utvikling av muskelproteiner og syntese av hormoner, enzymer og antistoffer. Industrielt produseres L-lysin ved en mikrobiell gjæringsprosess ved bruk av
Corynebacterium glutamicum . Hva er forskjellen mellom lysin og L-lysin? Lysin og L-lysin har samme fysiske egenskaper, bortsett fra retningen der de roterer polarisert lys. Som et resultat kan L-lysin ha vesentlig forskjellige biologiske effekter og funksjonelle egenskaper. Imidlertid er svært begrenset forskning gjort for å skille disse biologiske effekter og funksjonelle egenskaper. Noen av disse forskjellene kan omfatte, Smak
L-lysin:
L-former av aminosyrer pleier å være smakløse.
D-lysin:
D-former av aminosyrer har en tendens til å smake søtt. Derfor kan l-lysin være mindre / ikke søtere enn lysin.
Overflate L-lysin:
L-formene av aminosyre inkludert l-lysin er den mest omfattende form i naturen.Som et eksempel er ni av de nitten L-aminosyrer som vanligvis finnes i proteiner dextrorotatoriske og resten er levorotatoriske.
D-lysin:
D-formene av aminosyrer som ble observert eksperimentelt, viste seg å forekomme svært sjelden. Referanser: Solomons, T.W. Graham, og Graig B. Fryhle (2004). Organisk kjemi (8
th ed). Hoboken: John Wiley & Sons, Inc. Everhardus, A. (1984). Stereokjemi, grunnlag for sofistikert tull i farmakokinetikk og klinisk farmakologi, European Journal of Clinical Pharmacology, 26 , 663-668. Image Courtesy: "L-lysinmonokering-fra-hydroklorid-dihydrat-xtal-3D-baller" av Ben Mills - Egentlig arbeid via Wikimedia Commons




