Forskjell mellom IUPAC og fellesnavn | IUPAC vs fellesnavn
Nøkkelforskjell - IUPAC vs Fellesnavn
Navngivelse av kjemiske forbindelser er svært viktig for å sikre at talte eller skrevne kjemiske navn ikke gir noen forvirring, og et enkelt navn skal bare referere til ett enkelt stoff. IUPAC-navn følger et internasjonalt akseptert sett av regler , og alle kjemiske forbindelser får navn i henhold til disse reglene. I kontrast kan vanlige navn være ethvert navn som ikke har felles regler . Noen av IUPAC-navnene er svært vanskelig å huske, og det er veldig viktig å huske noen grunnleggende regler for å navngi kjemiske forbindelser. Folk er mer kjent med vanlige kjemiske navn enn deres IUPAC-navn, siden de fleste av de vanlige navnene er enkle å huske, og de inneholder ikke sifre, prefiks og suffiks . Dette er nøkkelforskjellen mellom IUPAC og Common Names.
Hva er IUPAC Navn?
IUPAC-navnene er den internasjonalt aksepterte metoden for å navngi kjemiske forbindelser. Generelt kan den videre deles inn i to hovedkategorier; uorganiske forbindelser og organiske forbindelser. Uansett hvor mange grener og hvor lenge molekylstrukturen er; IUPAC-navn kan brukes til å nevne et hvilket som helst område av molekyler. Men det er veldig vanskelig å nevne kjemiske forbindelser nøyaktig, uten å ha riktig kunnskap om disse reglene.

CaCO3 - Kalsiumkarbonat
Hva er vanlig navn på kjemiske forbindelser?
De vanlige navnene på kjemiske forbindelser følger ikke spesielle typer regler som i IUPAC-navn. Vanligvis er vanlige navn lett å huske og praktisk å bruke siden navngivningsmetoden ikke tar hensyn til molekylets, funksjonelle gruppers eller molekylersammensetning. Noen ganger har noen kjemikalier et enkelt navn for deres vanlige navn og for IUPAC-navnet.

CaCO3 - Kalkstein
Hva er forskjellen mellom IUPAC og fellesnavn?
Område:
IUPAC Navn: Hver kjemisk forbindelse får navn i henhold til IUPAC-nomenklaturen. IUPAC-navnet er direkte relatert til dets kjemiske struktur. IUPAC-navnene betegner med andre ord funksjonelle grupper, sidekjeder og andre spesielle bindingsmønstre i molekylet.
Eksempler:

I enkelte molekyler vurderer IUPAC-navn posisjonene der funksjonelle grupper befinner seg i molekylet.
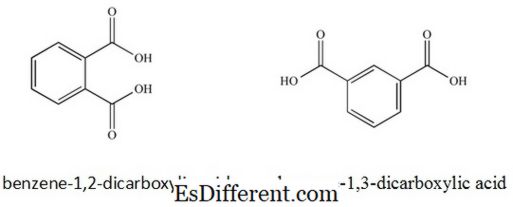
Eksempler:
- HCOOH - myresyre
- HCHO-formaldehyd
- C 6 H 6 - Benzen
- CH 3 COOH - eddiksyre Vanlige navn betrakter ikke posisjoner der funksjonelle grupper er festet.
Eksempler:

Uorganiske forbindelser:
- diff Artikkel Mellom før tabell ->
Formel| IUPAC Navn | Vanlig Navn | NaHCO |
| 3 Natriumbikarbonat Natriumhydrogenkarbonat | Baking soda NaBO | 3 |
| natriumperborat blekemiddel (fast) | Na | 2 |
| B 4 O 7 . 10 H 2 O natriumtetraborat, dekahydrat Borax | MgSO | 4 |
| . 2 2 2 Magnesiumsulfatheptahydrat Epsomsalt CF 2 Cl 2 | diklordifluormetan | Freon |
| PbS < bly (II) sulfid galena CaSO 4 | . 2 2 | O |
| kalsiumsulfatdihydrat | gips | Na |
| 2 S 2 O 3 | natriumtiosulfat < hypo | N |
| 2 O dinitrogenoksyd lattergas CaO kalsiumoksyd | kalk | CaCO |
| 3 kalsium karbonat kalkstein | NaOH | natriumhydroksyd |
| løye | Mg (OH) | 2 |
| magnesiumhydroksyd Magnesia-melk | SiO | 2 Silisiumdioksyd |
| kvarts | NaCl | natriumklorid |
| salt Organiske forbindelser: | Formel | IUPAC Navn |
| Fellesnavn CH 3 -CH = CH-CH | 3 | 2-buten |
| Symbutane | CH 3 | -CH (OH) -CH 3 |
2-propanol eller propan-2-ol




